El Premio Nobel de Química 2018 se otorgó el miércoles 4 de octubre a tres científicos que pusieron en marcha la evolución para diseñar moléculas a partir de organismos vivos que han llevado tanto al desarrollo de nuevos fármacos como de nuevos productos y procesos industriales de diversos tipos.
La Dra. Frances Arnold (https://www.che.caltech.edu/faculty/arnold_f), de Caltech, se ha llevado la mitad del premio de 1 millón de dólares. La Dra. Arnold ha desarrollado una técnica llamada evolución dirigida para generar proteínas y enzimas sintéticos. Comparte el honor con George Smith (https://biology.missouri.edu/people/?person=94), actualmente profesor emérito de la Universidad de Missouri, y Gregory Winter (https://www2.mrc-lmb.cam.ac.uk/group-leaders/emeritus/greg-winter), también emérito y líder de grupo en el Laboratorio de Biología Molecular (LMB) del Medical Research Council en Cambridge, UK. Smith y Winter han sido reconocidos por su trabajo en una técnica conocida como despliegue sobre fago, también en el campo de la evolución dirigida de nuevas proteínas, en particular, para la producción de anticuerpos de uso terapéutico.
El primer trabajo sobre la técnica, descrita por Smith en 1985 implica la introducción de ADN que codifica una proteína –un anticuerpo, por ejemplo- en un bacteriófago –un virus que infecta a las bacterias- El bacteriófago produce la proteína, que queda accesible sobre su superficie. Los investigadores pueden utilizar estos fagos, con proteínas específicas sobre su superficie, para estudiar su interacción con otras proteínas, con secuencias de ADN o con moléculas pequeñas.
Winter, cofundador de la compañía de biotecnología Cambridge Antibody Technology en 1989, desarrolló la técnica con el propósito de encontrar nuevas terapias. En 1993, su grupo de investigación utilizó el despliegue de fagos para aislar fragmentos de anticuerpos humanos que podrían unirse a antígenos específicos. Para obtener estos fragmentos los genes podrían expresarse en bacterias, y podrían ofrecer una «alternativa prometedora» a los métodos para la «producción de anticuerpos contra las moléculas de la superficie celular» basados en ratones.
En 2002, Adalimumab (Humira), un agente terapéutico producido por esta técnica, fue aprobado por las agencias europea y estadounidense para el tratamiento de la artritis reumatoide. En declaraciones en 2006, Winter calificó la aprobación como «el tipo de cosa de la que estoy más orgulloso». Desde entonces, la técnica se ha utilizado para aislar moléculas útiles contra enfermedades autoinmunes, diversos tipos de cáncer y bacterias como el Bacillus anthracis -la causa del ántrax-.
El Nobel concedido a Winter es el número 12 recibido por los investigadores del LMB en Cambridge. «Esta es realmente una gran historia sobre cómo la ciencia avanza desde la investigación básica hasta aquello que, en última instancia, está realmente comenzando a beneficiar a los pacientes», dice Phillip Holliger, un líder de programa en el LMB que trabajó con Winter, y añade «Creo que esa promesa se está cumpliendo, y es maravilloso verlo».
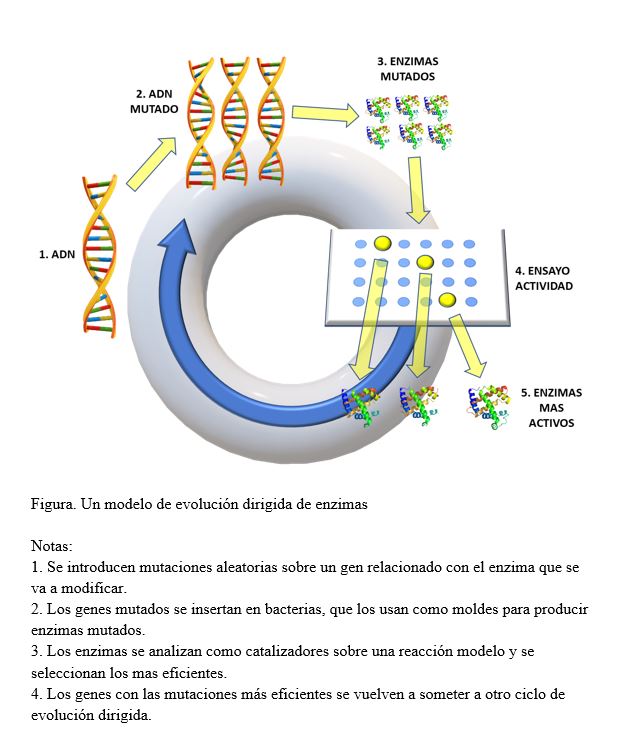
La evolución dirigida también se ha movido fuera del laboratorio a aplicaciones en diversos campos, sobre todo en la industria química. El trabajo pionero de Arnold para utilizar el principio de evolución para diseñar enzimas que realicen determinadas funciones, comenzó con una molécula llamada subtilisina E, una proteasa (enzima capaz de digerir proteínas). Arnold y su equipo utilizaron mutagénesis aleatoria para producir innumerables análogos de la enzima, luego seleccionaron aquellas con las propiedades deseadas, aplicaron sobre ellas la mutagénesis aleatoria nuevamente, y repitieron el proceso. Descrito en la revista PNAS en 1993, el equipo pudo producir una mutación de la subtilisina E 256 veces más eficiente que la natural, y a diferencia de esta, resistente además a entornos químicos agresivos. La subtilisina E y análogos se utilizan hoy en un gran número de productos de limpieza, detergentes, cosméticos, industria alimentaria, limpiadores de lentes de contacto, etc.
A lo largo de los años, Arnold ha continuado perfeccionando el método y aplicándolo a diferentes moléculas, creando incluso enzimas con funciones que no se ven en la naturaleza. Por ejemplo, en 2013, el equipo de Arnold desarrolló una enzima bacteriana modificada que puede producir ciclopropanos a través de un proceso que los organismos biológicos no habían realizado anteriormente.
La técnica se ha convertido en «muy ampliamente utilizada», comenta Lingchong You, biólogo de la Universidad de Duke, que hizo un postdoctoral con Arnold. «Se utiliza en todo tipo de disciplinas, incluyendo bioingeniería, química, biología, cuando las personas intentan usar esta técnica para optimizar una función precisa de interés en un enzima».
La evolución dirigida también ha tenido un gran efecto en la industria química, ayudando a desarrollar métodos de producción que sean más eficientes desde el punto de vista energético. En palabras de Volker Sieber, profesor de la Technische Universität München que fuese postdoctoral en el laboratorio de Arnold, «Los métodos desarrollados por Frances Arnold han sentado las bases para la producción de enzimas para una química más sostenible”.
Prof. Julio Alvarez-Builla G.
Dpto. de Química Orgánica. Universidad de Alcalá
Patrono y Consejero Científico de la Fundación GADEA por la Ciencia

