Un análisis de la calidad de los estudios registrados en el portal ClinicalTriasl.gov (portal en el que se debe registrar cualquier ensayo clínico cuyos resultados se pretendan publicar en una revista de prestigio) reveló que tan solo el 29% podrían alcanzar un grado de evidencia 2/5 según la escala de Oxford (siendo 1 el grado mayor y 5 el menor grado de evidencia) (30). Tan solo el 29% de los ensayos tenían estas dos características de bondad metodológica: (a) el grupo experimental se comparaba con un grupo control tratado con placebo, y (b) el desarrollo del estudio era “doble ciego” (tanto el paciente como el evaluador de los resultados desconocen si a cada sujeto se le administra el fármaco en estudio o placebo) (30).
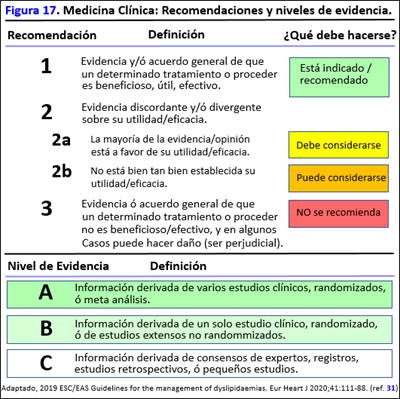
Para conseguir la mejor evidencia, la Medicina Clínica se ha dotado de instrumentos para graduar las recomendaciones de los expertos (generalmente grupos de expertos que redactan guías de práctica clínica) (Fig. 17) (31). Estas “recomendaciones” acerca de lo que se debe hacer y no hacer se basan en estudios clínicos, no siempre concordantes, que pueden tener metodologías muy diversas y cuya información (evidencia) se puede graduar en tres niveles (A, B y C) (Fig. 17).
Un ejemplo ilustrativo se recoge en la figura 30. Podemos graduar la “evidencia” de las recomendaciones ofrecidas por un consenso de expertos para el tratamiento farmacológico de pacientes con colesterol elevado, según los estudios hoy disponibles (Fig. 18) (31).

Los investigadores clínicos disponen de muchas guías para realizar su actividad investigadora con el esmero y detalle pretendidos (32).
Naturalmente, estos esfuerzos y sus consecuciones son muy dependientes de los recursos humanos y económicos disponibles, que casi nunca son los óptimos, ni siquiera en las circunstancias tan delicadas en las que estamos.
En nuestro entorno, la Directora del Instituto de Salud Carlos III ha dicho: “El médico que investiga lo hace en su tiempo libre; es heroico, pero insostenible” (33).
Para hacernos una idea del esfuerzo investigador que está realizando la comunidad biomédica mundial, considere el lector esta cifra: en los 57 días comprendidos entre el 5 de julio y 31 de agosto 2020 se han publicado en PubMed (el buscador de publicaciones biomédicas más utilizado en el mundo) 315 publicaciones cada día, es decir más de 9.000 estudios cada mes (34).
06/09/2020 – Dr. Juan García Puig
Para responder bien a esta pregunta debemos considerar varias premisas. La Medicina no es una ciencia exacta. El conocimiento se genera a partir de investigaciones que se realizan en laboratorios, consultas, hospitales que, por definición, atienden a un conjunto de personas limitado, de no todas las edades, razas, áreas geográficas, etc. Los datos de las investigaciones son interpretados por personas, que tienen intereses diversos. La diseminación de los resultados suele realizarse a través de publicaciones biomédicas, tras una revisión por expertos de cada área del conocimiento / especialidad, que también tienen intereses propios (expertos y editores de revistas). Los hallazgos y aportaciones relevantes suelen ser verificados por otras investigaciones, que no siempre llegan a las mismas conclusiones … y con frecuencia se requieren nuevos estudios para intentar responder a las preguntas planteadas.
El rigor científico en estos meses de pandemia ha estado muy comprometido por diversos factores: población afectada en más de 190 países, abrumadora morbilidad y mortalidad que demandaba soluciones urgentes, crisis económica de dimensión planetaria, etc.
La URGENCIA para disponer de fármacos efectivos contra la Covid-19 ha motivado la elaboración de publicaciones apresuradas, tal vez poco elaboradas, sin el rigor suficiente y habitual de las investigaciones biomédicas. Estas prisas, en ocasiones, han dado lugar a investigaciones de muy baja calidad, con errores metodológicos, que han ofrecido datos confusos, poco fiables. También debemos aceptar que los ensayos –todas las investigaciones– tienen “limitaciones”, entre otras razones porque ningún estudio en humanos puede abarcar todos los continentes, todos los estratos de edad, razas, niveles socioeconómicos, … y las respuestas siempre son “parciales ó limitadas a esa población del estudio”.
Un ejemplo ilustrativo es la historia del fármaco remdesevir. Este fármaco antiviral (empresa Gilead) ha sido estudiado en tres ensayos clínicos muy difundidos. Parece que tiene cierta utilidad para disminuir la estancia hospitalaria de los pacientes con Covid-19, el porcentaje de ingresos en las UCI y la mortalidad. Tras un análisis detallado de los tres estudios, no sabemos con precisión (26): (a) la población que más se puede beneficiar de su administración, (b) la duración más adecuada del tratamiento, (c) su eficacia cuando se administra con / sin dexametasona / corticoides. Los tres ensayos con remdesevir se realizaron antes de que se conocieran los resultados del estudio RECOVERY (la administración de dexametasona se asoció a una reducción de la mortalidad en pacientes Covid-19 graves, pero no en los enfermos que no requirieron oxígeno suplementario [27], lo que se ha confirmado en otros estudios y un metaanálisis publicado el 2 de septiembre [28]).
“La infoxicación es un consustancial a nuestro tiempo”, ha dicho Eva Méndez, presidenta de la Open Science Policy Platform de la Comisión Europea. “Creo en el rigor de la ciencia y en la capacidad del sistema científico de corregirse y de que la comunidad dirima lo que es válido”, y ha añadido “En estos tiempos, el parámetro tiene que seguir siendo la excelencia” (29).

Un análisis de la calidad de los estudios registrados en el portal ClinicalTriasl.gov (portal en el que se debe registrar cualquier ensayo clínico cuyos resultados se pretendan publicar en una revista de prestigio) reveló que tan solo el 29% podrían alcanzar un grado de evidencia 2/5 según la escala de Oxford (siendo 1 el grado mayor y 5 el menor grado de evidencia) (30). Tan solo el 29% de los ensayos tenían estas dos características de bondad metodológica: (a) el grupo experimental se comparaba con un grupo control tratado con placebo, y (b) el desarrollo del estudio era “doble ciego” (tanto el paciente como el evaluador de los resultados desconocen si a cada sujeto se le administra el fármaco en estudio o placebo) (30).
Para conseguir la mejor evidencia, la Medicina Clínica se ha dotado de instrumentos para graduar las recomendaciones de los expertos (generalmente grupos de expertos que redactan guías de práctica clínica) (Fig. 17) (31). Estas “recomendaciones” acerca de lo que se debe hacer y no hacer se basan en estudios clínicos, no siempre concordantes, que pueden tener metodologías muy diversas y cuya información (evidencia) se puede graduar en tres niveles (A, B y C) (Fig. 17).
Un ejemplo ilustrativo se recoge en la figura 30. Podemos graduar la “evidencia” de las recomendaciones ofrecidas por un consenso de expertos para el tratamiento farmacológico de pacientes con colesterol elevado, según los estudios hoy disponibles (Fig. 18) (31).

Los investigadores clínicos disponen de muchas guías para realizar su actividad investigadora con el esmero y detalle pretendidos (32).
Naturalmente, estos esfuerzos y sus consecuciones son muy dependientes de los recursos humanos y económicos disponibles, que casi nunca son los óptimos, ni siquiera en las circunstancias tan delicadas en las que estamos.
En nuestro entorno, la Directora del Instituto de Salud Carlos III ha dicho: “El médico que investiga lo hace en su tiempo libre; es heroico, pero insostenible” (33).
Para hacernos una idea del esfuerzo investigador que está realizando la comunidad biomédica mundial, considere el lector esta cifra: en los 57 días comprendidos entre el 5 de julio y 31 de agosto 2020 se han publicado en PubMed (el buscador de publicaciones biomédicas más utilizado en el mundo) 315 publicaciones cada día, es decir más de 9.000 estudios cada mes (34).

